ステロイドはステロイド環を基本骨格にもつ化合物の総称ですが、この中にはコレステロールをはじめ、ステロイドホルモン、胆汁酸など生理的に重要な物質が含まれます。そのためステロイドは様々な分野でとても重要なテーマの一つでもあります。といっても構造は複雑だし、生合成経路はややこしいし、よくわからないですよね。そこで今回はステロイドの基礎から生合成経路、代謝や誘導体について解説していきます。
Contents
ステロイドの定義と概要
ステロイド環の構造と番号の割り振り方は?
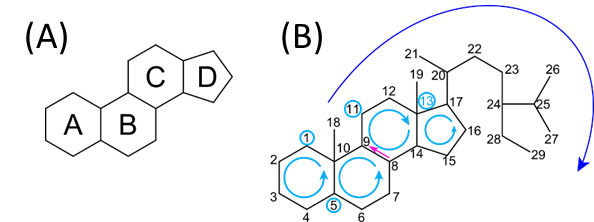
ステロイドとはその名の通りステロイド環を持つ化合物の総称です。ステロイド環というのは図1の (A) に記載しているような構造のことを言います。ステロイド環は六員環が三つと五員環が一つで構成されていますが、それぞれの環について左からA、B、C、Dと名前が付けられています(いろいろな化合物の中で見ると複雑に見えますが、ステロイド環だけを見るとわかりやすいと思います。まずはこの形を覚えましょう)。さらに置換基のつく位置を特定するために各炭素に番号を割り付けます。その割り付け方は図1の (B) に示しています。番号の付け方はまず、A~Dの環の番号を割り付けます。A、Bの環は反時計回りに番号を付けます。8 と 9 について注目してください。この位置を C の環から見ると番号が時計回りになっていますね。なので、C については時計回りに番号をつけましょう。すると 13 と 14 は D の環から見ると反時計回りになっていますので D の環は反時計回りに番号をつけましょう。次に残った側鎖について、番号を付けていきます。側鎖の番号は A ~ D の順につけていきます(濃い青矢印)。そうすると、図1の (B) のような番号の付け方になります。
ステロイドの立体構造には二種類ある
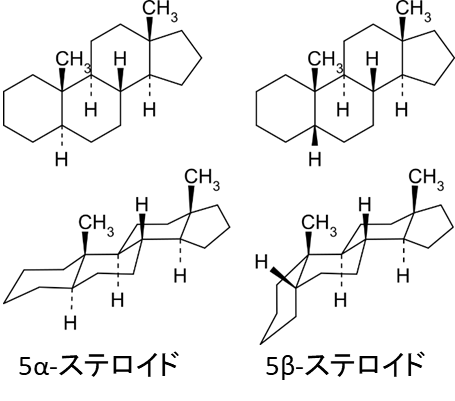
ステロイド環の立体構造はどうなっているのでしょうか?構造については図2を参考にしてください。A~Cの環についてはすべていす形の配座をとっています。BとCの関係はどちらの立体構造でも同じ配置をとります。ですが、AとBの関係については二種類あります。一つは図2の左側に示したようにAの椅子の形が横向きになるような配置です。この時5位の水素が画面の後ろ向きに配置します(点線は画面に対して奥方向に向かっていることを意味します)。この構造は 5α-ステロイドといいます。もう一つは図2の右側に示したようにAの椅子の形が縦向きになるような配置です。この時5位の水素が画面の手前向きに配置します(太線は画面に対して手前方向に向かっていることを意味します)。この構造は 5β-ステロイドといいます。
最も代表的なステロイド、ステロール
ステロール (sterol) というのはステロイド環を持つ一価アルコール(水酸基を一つ持つ)のことを言います。この水酸基は3位の炭素に配置する場合がほとんどで、17 位に炭素数 8 ~ 10 個程度の側鎖を持つ場合も多いです。ステロールでもっとも代表的なものはコレステロール (cholesterol) です。コレステロールの概要を以下に記載しますね。
- 体内でスクアレンから合成される
- 最も代表的なステロール
- 胆汁酸の生合成の出発物質(胆汁酸の元となる物質)
- 動脈硬化・胆石の生成の原因物質
では、次からはコレステロールについてみていきましょう。
コレステロールの生合成経路と生合成の制御
コレステロールは動物に広くみられる物質で、脂質の消化に重要な胆汁酸や細胞膜の構成要素、ステロイドホルモンなど様々な場面で重要な役割を担っている物質です。コレステロールは食べ物にも含まれているので外から吸収するものもありますが、体内でも生合成が可能です。この生合成経路は一見とても複雑そうに見えますが、順を追ってみていくとそれほど煩雑ではありません。ここではコレステロールの生合成経路について解説していきます。さらにコレステロール生合成は厳密な制御を受けていますが、この制御についても解説していきますね。
コレステロールの生合成は3段階で進む
コレステロールは成人で一日あたり 800 mg 合成されます。コレステロールの合成はどこでも行われるわけではなく、腸と肝臓で行われます。したがってこれらの臓器から全身へ運搬するメカニズムも存在します。この点については別記事で解説します。生合成はアセチルCoA が出発物質として ATP や NADPH を消費して進みます。では合成経路についてみていきましょう。
コレステロールの生合成は複雑そうに見えますが、整理して理解するとそれほどでもないので落ちついて確認していきましょう。まず、コレステロールの生合成の合成段階を三つに分けて考えましょう。
- イソペンテニル二リン酸の合成
- イソペンテニル二リン酸が縮合してスクアレンを合成
- スクアレンの環化によりコレステロールを合成
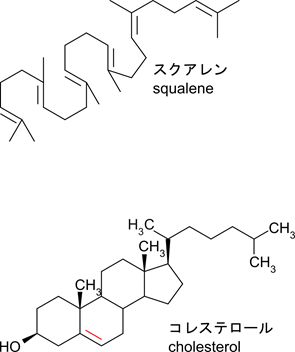
右の構造式を見てください。スクアレンの構造とコレステロールの構造を見比べてみてほしいのですが、これらの構造がよく似ていることに気付くかと思います。実はスクアレンの数カ所が架橋されただけでコレステロールに似た構造を持つラノステロールが合成されます。その後ラノステロールがコレステロールに変換されるという経路をたどります。ということはコレステロールの生合成のためにはスクアレンを合成することが必要になります。さて、スクアレンはイソプレノイドに分類される物質です。この辺については ”イソプレンの組み合わせで構成されるテルペン類 (イソプレノイド)” という記事で詳細に解説していますので、ぜひ読んでみてください。
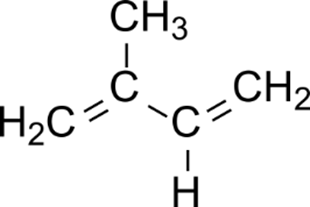
スクアレンは右に示したイソプレンという構造の組み合わせでできています。ですので、まずはイソプレンに似た構造を持つ物質を形成することが1段階目となります。実際、この段階で合成されるイソペンテニル二リン酸とジメチルアリル二リン酸はテルペン類の前駆物質です。この反応はさらに2段階に分けて考えるとわかりやすいと思います。
- メバロン酸の合成
- メバロン酸からイソペンテニル二リン酸の合成
以下に反応の内容について解説します。
1.イソペンテニル二リン酸の合成ステップ
メバロン酸の合成
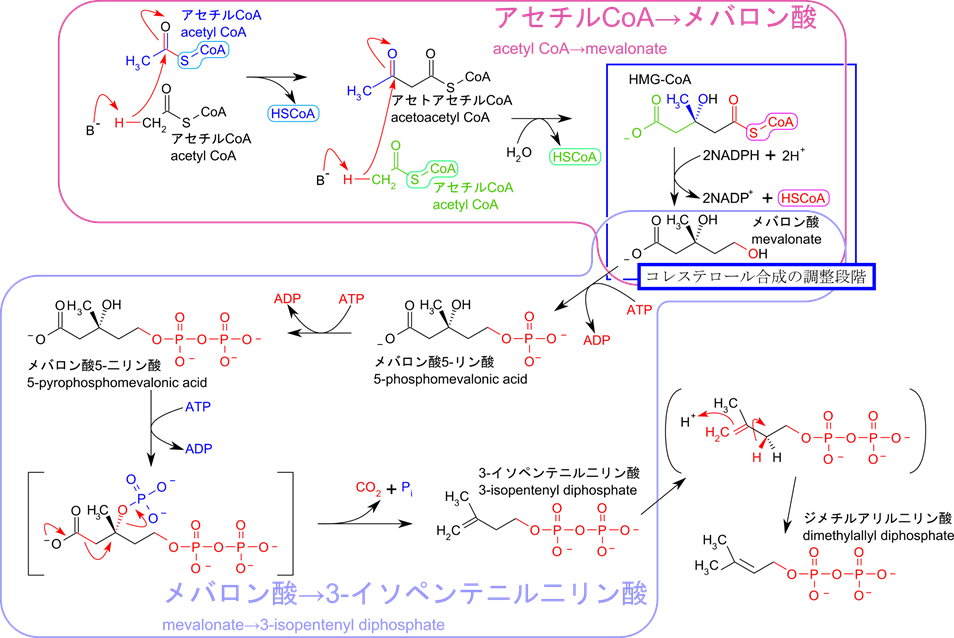
出発物質はアセチルCoAですが、アセチルCoAが重合してアセトアセチルCoA になります。さらに、アセチルCoA がアセトアセチルCoA と重合してヒドロキシメチルグルタリルCoA (hydroxymethylglutaryl CoA; HMG-CoA) が生成されます。この HMG-CoA から補酵素A (CoA) が切断されるとメバロン酸になります。メバロン酸を生成するステップはヒドロキシメチルグルタリル CoA レダクターゼ〔hydroxymethylglutaryl CoA reductase;HMG-CoA reductase〕 によって制御されています。この酵素はコレステロール合成にとってとても大切な段階で、コレステロールが豊富にある場合、この HMG-CoA が制御を受けることで合成系が停止します(この解説は後述します)。
メバロン酸からイソペンテニル二リン酸の合成
メバロン酸が合成されるとリン酸化を受ける段階に進みます。このステップではメバロン酸がリン酸化を受けるとともに、炭酸が抜き取られて 3-イソペンテニル二リン酸が合成されます。この時にATP を消費します。合成されたイソペンテニル二リン酸は図3ー1の右下に描いたような異性化(異性体への変換)を経てジメチルアリル二リン酸に変換されます。次の反応ではイソペンテニル二リン酸とジメチルアリル二リン酸が出発物質となります。まだまだ、コレステロールの構造のかけらも見えませんね。ですが、これらの分子が結合しあってスクアレン次いでコレステロールが形成されていきます。ではそのステップを見ていきましょう。
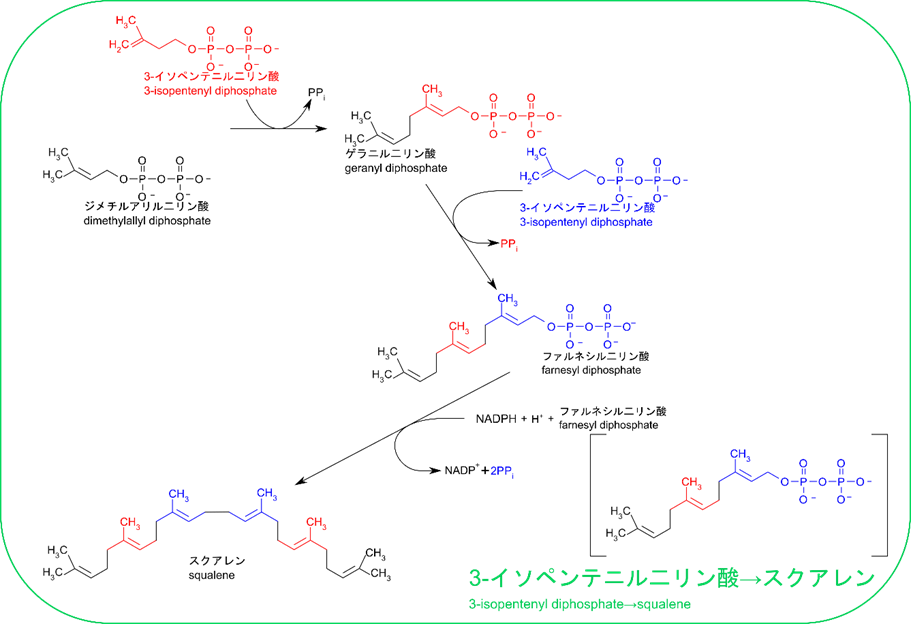
2.イソペンテニル二リン酸が縮合してスクアレンを合成
図3-2を見てください、ここでは合成されたイソペンテニル二リン酸が縮合してスクアレンを合成するステップを示しています。まずは炭素数に注目して合成経路を見てみましょう。イソペンテニル二リン酸は炭素数5個の構造ですね。これが二つ縮合するとゲラニル二リン酸になります。炭素数は10個の構造ですね。炭素数から見ても二つのイソペンテニル二リン酸が重合していることがわかると思います。ここにもうひと分子のイソペンテニル二リン酸が重合するとファルネシル二リン酸が合成されます。炭素数は15個です。イソペンテニル二リン酸が3分子分ですね。このファルネシル二リン酸が二分子重合してスクアレンになります。スクアレンは炭素数は30個ですね。さて、これまで炭素数を数えていましたが、これには理由があります。イソペンテニル二リン酸あるいはジメチルアリル二リン酸はイソプレン一分子分の構造です。これが二つ結合するとゲラニル二リン酸となります。この分子はゲラニオールにリン酸が二分子結合した構造になっていますが、ゲラニオールというのはモノテルペンの一種です。モノテルペンはテルペンの内、炭素数 10 個のものでしたね。さらに合成されるファルネシル二リン酸はファルネソールにリン酸基が結合した構造ですね。ファルネソールというのはセスキテルペン(テルペンの内、炭素数15個)の一種です。最後にスクアレンが合成されますが、スクアレンはテルペンの内、炭素数30個のテルペンでトリテルペンと呼ばれます。つまり、この過程はイソプレン単位が縮合してモノテルペン→セスキテルペン→トリテルペンとなっていく過程となっていることがわかりますね。
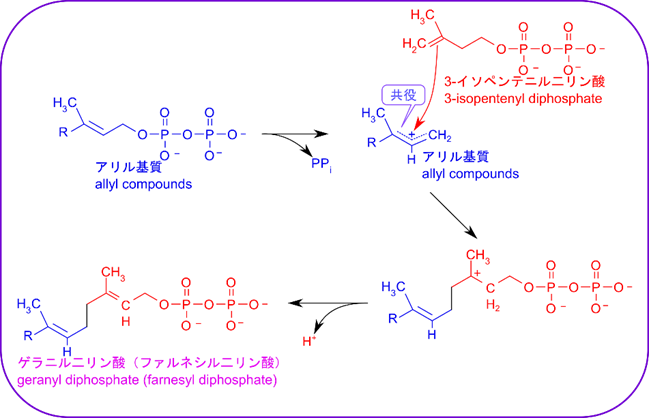
全体の流れを見てみた後は個々の反応についてみてみます。図3-2の Supplement を見てみましょう。まずはアリル基質からリン酸基が脱離します。するとリン酸が結合していた炭素に空の電子軌道が一つできますね。この軌道を利用して π 電子が共鳴構造をとります。すると図3-2(supplement)のように炭素原子が(少し電子が足りない状態になるので)プラスに偏ります。ここをイソペンテニル二リン酸の π 電子が攻撃して結合します。その結果イソペンテニル二リン酸中に電子が足りない炭素原子(結合の手が3本しかないですね。ということは電子軌道が一つ余っているということですが、このことは電子が足りていないということでもあり、原子全体としてみればプラスに偏っていることになります)ができます。この状態をカルボカチオンといいます。さらにプロトンが脱離することで(水素原子が電子をおいてプロトンとして脱離することで)、カチオンに電子を供給してゲラニル二リン酸やファルネシル二リン酸が合成されます。図3ー2の合成経路はこの反応の繰り返しになっています。
さて、こうしてスクアレンが合成されました。これでだいぶコレステロールに近づいてきましたね。次はいよいよコレステロールが合成されます。では最後の段階を見ていきましょう。
3.スクアレンの環化によりコレステロールを合成
図3-3を見てください。最初の構造がスクアレンの構造です。図3ー2の最終産物と違う!といわないでくださいね。端から順番に結合のパターンを追ってみてください。同じ構造になっていることがわかると思います。こうしてみると少し架橋してやるとコレステロールに近い構造になりそうですね。この架橋形成の経路がこの合成経路になります。さて、まずは左端の二重結合に酸素が結合して環状構造を形成します。するとこの足元の炭素原子に二重結合の π 電子が遷移して結合を形成します。次にドミノ倒しのように順次 π 電子が遷移して結合を形成していきます。こうしてプロトステロールカチオンを形成します(青矢印の通りです)。今度はプロトンが脱離して電子がカチオン部分に遷移するとともに、順次各置換基が遷移していきます(緑矢印の通りです)。こうしてできた分子はラノステロールという分子です。ここからコレステロールまでの経路はかなり複雑ですので省略しますが、青で示したメチル基が脱離してコレステロールに変換されます。こうして無事コレステロールが合成されました。

さて、こうして得られたコレステロールは細胞膜の構成要素になったり、ステロイドホルモンの基本骨格になります。さて次は合成の制御についてみていきましょう。
コレステロールの合成制御はHMG-CoA レダクターゼに対して様々なレベルで行われる
タイトルに ”様々なレベルで” と書きました。この意味は何でしょう?以下に列挙してみます。
- HMG-CoA レダクターゼ mRNA 合成制御
- HMG-CoA レダクターゼ mRNA 翻訳制御
- HMG-CoA レダクターゼ分解制御
- HMG-CoA レダクターゼ活性制御
さて、タンパク質の一生を簡単に考えてみましょう。
- 遺伝子発現から mRNA の合成
- mRNA が翻訳されてタンパク質が合成される
- 翻訳語修飾が行われて様々な修飾を受ける
- 適切な位置に輸送されて(あるいは分泌されて)機能する
- 最終的に分解されて消滅する
HMG-CoA レダクターゼが調節を受けるレベルを赤字で示しています。いかがですか?かなり厳重に制御されていることがわかるかと思います。では順番に見ていきましょう。
HMG-CoA レダクターゼ mRNA 合成制御
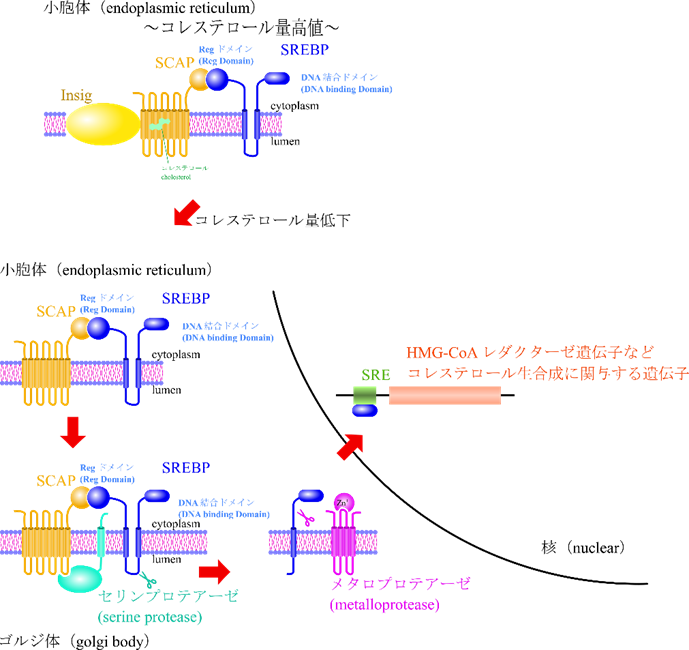
この制御はコレステロールの量に応じてHMG-CoA レダクターゼ遺伝子の on/off が切り替わることで行われます。つまり、この遺伝子の on/off の切り替えを行うメカニズムがこれから解説する内容になります。この内容は図4に示していますので図4と比べてみながら読んでみてください。
コレステロールレベルは SREBP 切断活性化タンパク質 (SREBP cleavage activating protein; SCAP) により感知されています。つまり SCAP というのはコレステロールセンサーと考えてください。ちなみに SREBP は次に出てきますのでここでは何かの因子と思ってください。SCAP は細胞内コレステロール量がある一定量以上であるとコレステロールと結合しており、 Insig (Insulin induced gene) と結合しています。Insig はアンカーであり、まさに船のいかりのように SCAP や SREBP を固定する役割を担っています。
コレステロールレベルが低くなると SCAP からコレステロールが脱離して構造変化が生じ、Insig が外れます。コレステロールが多いと容易にコレステロールと結合できますが、周りのコレステロールが減少するとバランスをとるために放出するというイメージを持っていただけるとわかりやすいかと思います。すると SCAP はステロール調節エレメント結合タンパク質 (sterol regulatory element binding pretein; SREBP) をゴルジ体へ移行させます。この過程は SCAP が輸送小胞上のタンパク質と結合することによりコントロールされています。ゴルジ体へ移行するとセリンプロテアーゼによる加水分解を受けて SREBP の一部が SCAP から離れます。次にメタロプロテアーゼによる加水分解により SREBP の DNA 結合ドメインが遊離して、核へと移行してステロール調節エレメント (sterol regulatory element; SRE) に結合します。そのことがスイッチになって HMG-CoA レダクターゼのようなコレステロール合成にかかわる遺伝子の発現が促進されます。
一方でコレステロールレベルが高くなると、SREBP の切断による遊離が阻害され、核内の SREBP の DNA 結合ドメインがプロテアソームにより分解されることでコレステロール合成にかかわる遺伝子の発現が阻害されます。一方で前述したようにコレステロールと結合している SCAP が Insig と結合することにより SREBP のゴルジ体への移行を制御しています。
HMG-CoA レダクターゼ mRNA 翻訳制御
この制御メカニズムはメバロン酸由来の非ステロール代謝産物が mRNA 翻訳速度を抑制することにより行われます。この現象については例えば、培養細胞にメバロン酸を添加した場合、HMG-CoA レダクターゼの量が減少して mRNA の量が変わらないということが報告されています。
HMG-CoA レダクターゼ分解制御
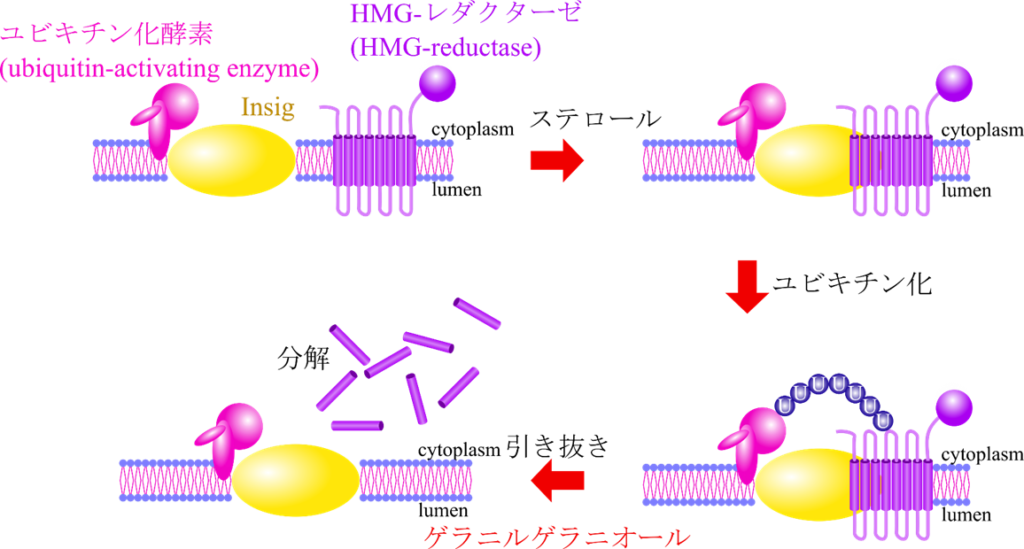
HMG-CoA レダクターゼの細胞質ドメイン(外側)は触媒作用を、膜ドメイン(膜に埋まっている領域)は酵素の分解をもたらすシグナルを受け取る役割を担っています。膜ドメインがステロール類(ラノステロール、25-ヒドロキシコレステロール)の濃度上昇を感知すると構造変化を起こして、Insig に結合します。するとユビキチン化酵素と結合してこの酵素の作用によりポリユビキチン化を受けます。ユビキチン化は目印をつけていると理解してくれるとわかりやすいと思います。この目印を見極めてゲラニルゲラニオールを要求する過程で膜から引き抜かれて、プロテアソームにより分解されて HMG-レダクターゼは消滅します。ここで出てきたゲラニルゲラニオールというのはイソペンテニル二リン酸とファルネシル二リン酸の縮合により生成される物質です。
HMG-CoA レダクターゼ活性制御
HMG-レダクターゼはリン酸化を受けるとと活性が低下します。この過程は AMP 依存性プロテインキナーゼ(AMPで活性化、ATP で阻害されるキナーゼ)によって行われます。AMP 依存性プロテインキナーゼは燃料計のような役割を担っています。ATP というと生物の燃料みたいなものですね。AMP イオン性プロテインキナーゼは ATP の量の多い、少ないを検知して脂質代謝や脂質合成を制御する役割を担っています。ここでも ATP 量が少ない場合には HMG-CoA レダクターゼのリン酸化が促進されて活性が低下するので、コレステロール合成が起こらなくなります。
脂質消化を助ける胆汁酸
脂質は疎水性の分子であるためにそのままでは消化が難しい物質です。そこで活躍するのが胆汁酸です。胆汁酸はコレステロールの極性誘導体です。つまり図6の左端に構造の “R” の部分に極性を持つ分子が結合した形をしています。この結果、ステロール環の疎水性部分と側鎖の親水性部分を持つのでとても有効な界面活性剤(detergent)として機能します。代表的な胆汁酸はコール酸(”R” の部分が水酸基)ですが、遊離状態で存在することはレアで、実際は他の分子と結合しています。グリシン(glycine)と結合しているグリココール酸、タウリン(taurine)と結合しているタウロコール酸が代表的です(図6)。
胆汁酸は肝臓で合成され、胆のうに貯蔵・濃縮されます。その後、小腸に放出されて脂質の消化を促進します。胆汁酸は界面活性剤ですので、脂質を可溶化させることが主な役割です。この可溶化の結果、脂質の有効面積が増大して
- 表面積が大きくなり、リパーゼの作用が大きくなる
- 小腸からの消化が容易になる
という利点をもたらします。

左端の構造の “R” が水酸基ならコール酸、タウリンならタウロコール酸、グリシンならグリココール酸となります。
ステロイドホルモン、性ホルモンと副腎皮質ホルモン
ステロイドはある種のホルモンも含みます。ホルモンというのはいろいろな細胞に情報を伝達する物質です。体内のいろいろな組織や細胞は適切なときに適切な機能を果たす必要があります。これを統制するために情報を媒介する物質が分泌されます。これらの物質は受け取るべき細胞が受け取ることでこの物質が伝えている情報に従って決まった機能を果たします。このようにホルモンは生体が正しく機能するためにとても大切な物質です。
副腎皮質ホルモン
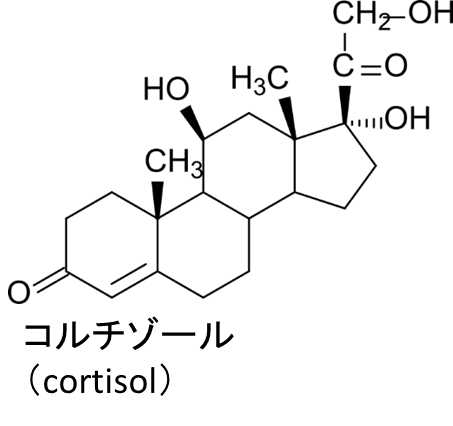
代表的な副腎皮質ホルモンの一つにグルココルチコイド (glucocorticoid) があります。グルココルチコイドは糖新生の促進、脂肪とタンパク質の分解促進、抗炎症作用を持ち、動物のストレス応答を誘導するなど生体の恒常性の維持に重要な働きを持っています。代表的なグルココルチコイドはコルチゾール (cortisol; 図7) です。
ここで糖新生について確認しておきます。激しい運動をしたときに腕や足がつったことはないでしょうか?このようなときには乳酸発酵が進み、乳酸が大量に産生されます。この乳酸は肝臓に運ばれてグルコースやグリコーゲンの合成に使われます。この過程を糖新生といいます。この過程が促進されるということは、糖を貯蔵形態に変換することになるので、糖の利用を低下させ、血糖を上昇させる(インスリンの作用と拮抗)ことになります。
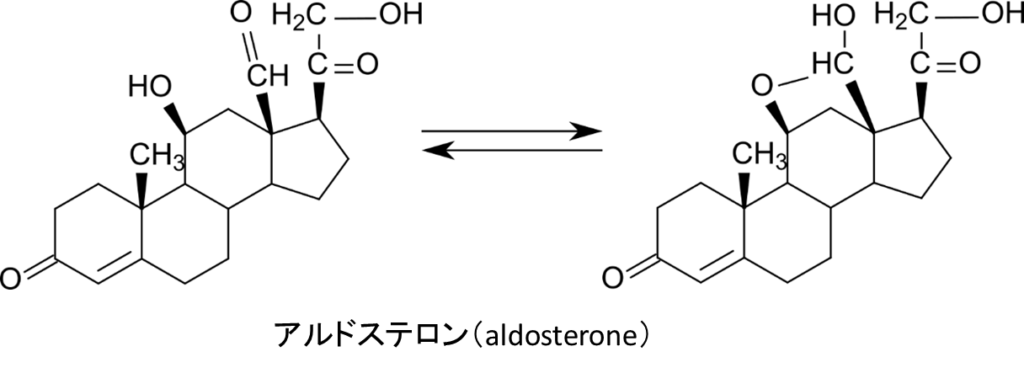
ミネラルコルチコイド (mineral corticoid) も代表的な副腎皮質ホルモンです。腎臓の遠位尿細管(尿を希釈する組織)に作用して、Na+ の再吸収と K+ と H+ の排出を促進して血液量が増加し血圧が上昇します。代表的なミネラルコルチコイドはアルドステロン(aldosterone; 図8)があります。
性ホルモン
性ホルモンは二次性徴の発現を誘導し、生殖器の成長発達を促進します。ステロイドホルモンには性ホルモンも含まれており、様々な機能を発揮しています。
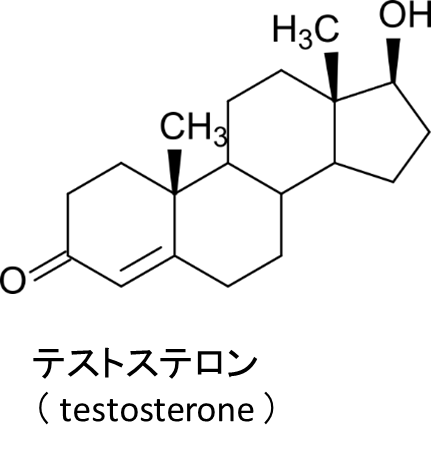
テストステロン(testosterone; 雄性ホルモン)
テストステロンはその名の通り、雄性生殖器の発達を誘導して、オスの身体的特徴を発現・維持することが役割となります。テストステロンは脳内で作用し、オスの性行動の発達に関与しています。さらにステロイド 5α-レダクターゼの作用により還元されるとジヒドロテストステロン (dihydrotestosterone, DHT) に変換されますが、DHT は雄性表現型への発達と分化を促す強力な胎生期のホルモンです。
エストロゲン(雌性ホルモン)
エストロゲンは、雌性生殖器の発達を誘導することが機能です。大きく分けて二つに分類できます。
一つ目はメスの身体的特徴を発現・維持するもので、卵胞ホルモンと呼ばれます。代表的なものには以下の三つが含まれます。
- エストロン(estrone)
- エストラジオール(estradiol)
- エストリオール(estriol)
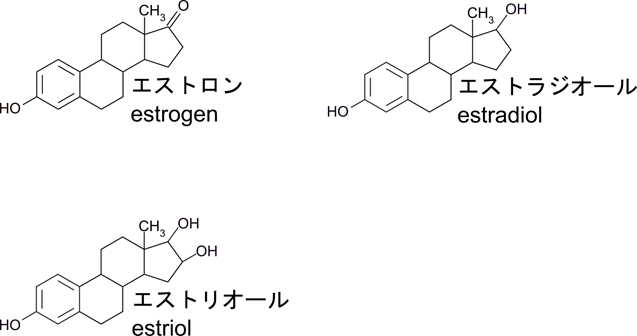
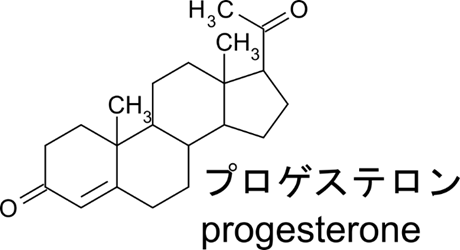
もう一つは子宮内膜の状態を維持して、乳汁の分泌を促進するもので、黄体ホルモンと呼ばれます。代表的なものにはプロゲステロン (progesterone) が含まれます
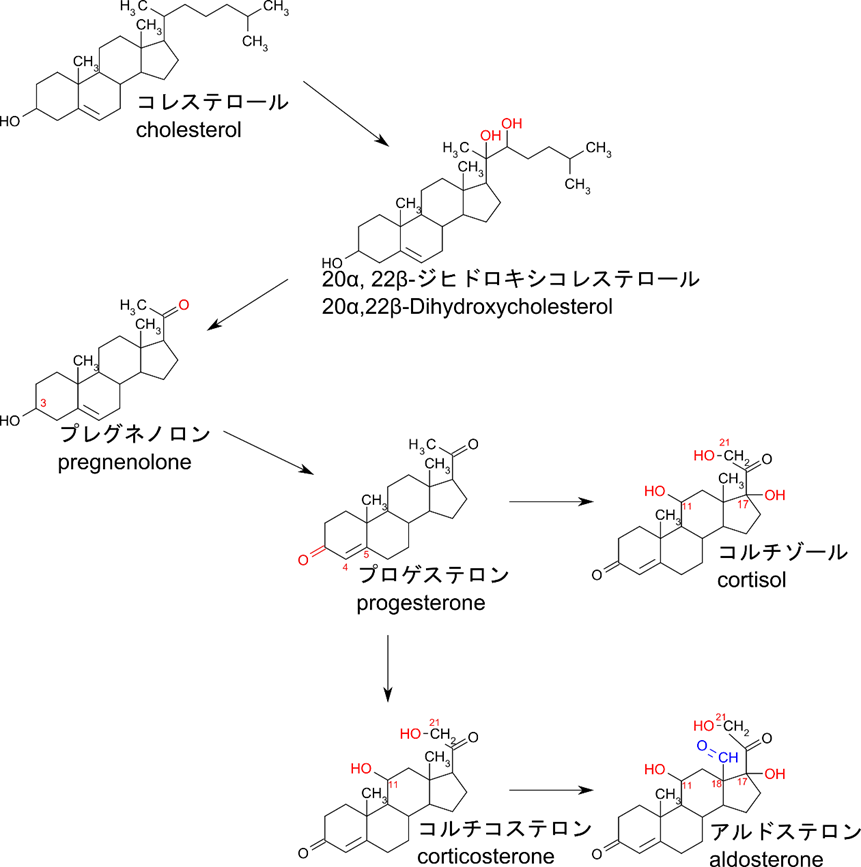
ステロイドホルモンの生合成経路
黄体ホルモンであるプロゲステロンと副腎皮質ホルモンであるコルチゾール、アルドステロンの生合成経路を見ていきましょう。出発物質はコレステロールですね。コレステロールの 20 位、次いで 22 位の炭素がヒドロキシ化されて 20α, 22β-ジヒドロキシコレステロールを生成します。次に 20 位の炭素と 22 位の炭素の間で切断されてプレグネノロンが生成されます。このプレグネノロンが様々なステロイドホルモンの前駆体となります。まず 3 位の水酸基が酸化されるとオキソ基(=O)に変換されるとともに、Δ5 二重結合(5-6 位間の二重結合)は Δ4 二重結合(4-5 位間の二重結合)に変換されます。そうするとプロゲステロンが合成されました。さらに11 位、17 位、21 位の炭素がヒドロキシ化されるとコルチゾールになります。一方でプロゲステロンの 21 位の炭素が、次いで 11 位の炭素がヒドロキシ化されるとコルチステロンが合成されます。このコルチステロンがアルドステロンの前駆体です。さらに 18 位のメチル基が酸化されてアルデヒド基になると同時に 17 位の炭素がヒドロキシ化するとアルドステロンとなります。
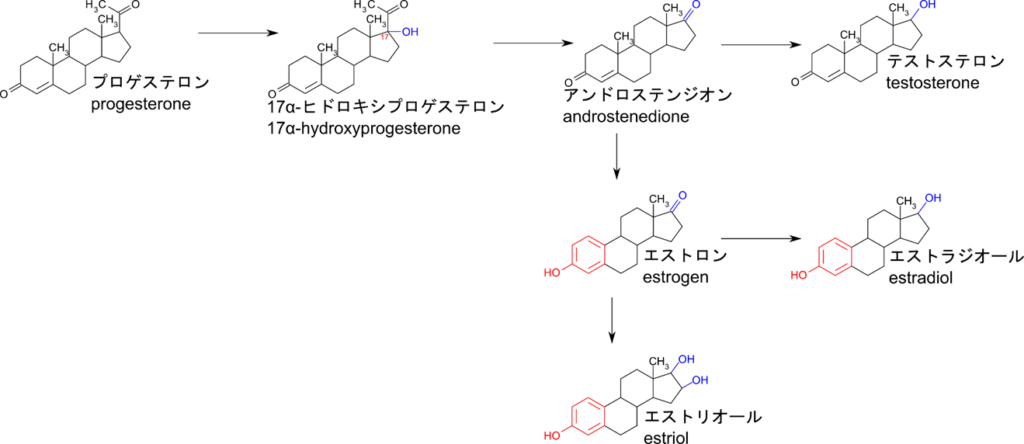
次に各種性ホルモンの合成経路についてみていきましょう。この時の出発物質はプロゲステロンです。まず 17 位の炭素がヒドロキシ化されて 20、21 位の炭素からなる側鎖が切断されるとアンドロステンジオンが合成されます。アンドロステンジオンの 17 位のオキソ基が還元されるとテストステロンになります。一方でアンドロステンジオンの 3 位のオキソ基が還元されて水酸基に、また 19 位のメチル基が切断されることでエストロンとなります。次に 17 位のオキソ基が還元されるとエストラジオールに、一方で 17 位のオキソ基の還元とともに16 位の炭素がヒドロキシ化されるとエストリオールとなります。
今回はステロイドについて概説してみました。ここに記載したほかにもビタミンD 群の合成前駆体になるなど重要な物質として知られています。気になる方はぜひ調べてみてください。最後まで読んでいただいてありがとうございました。
参考文献
- 島原健三 (1991). 概説 生物化学. 三共出版. pp. 67-84
- Jeremy M. Berg, John L. Tymoczko, Gregory J. Gatto Jr., Lubert Stryer著、入村達郎、岡山博人、清水孝雄、中野徹訳 (2018). ストライヤー生化学 第8版. 東京化学同人. pp. 718-750
- DeBose-Boyd, R. A. (2008). Feedback regulation of cholesterol synthesis: Sterol-accelerated ubiquitination and degradation of HMG CoA reductase. Cell Research, 18(6), 609–621.
- Nakanishi, M., Goldstein, J. L., & Brown, M. S. (1988). Multivalent control of 3-hydroxy-3-methylglutaryl coenzyme A reductase. Mevalonate-derived product inhibits translation of mRNA and accelerates degradation of enzyme. Journal of Biological Chemistry, 263(18), 8929–8937.
- Sagami, H., Korenaga, T., & Ogura2, K. (1993). Geranylgeranyl Diphosphate Synthase Catalyzing the Single Condensation between Isopentenyl Diphosphate and Farnesyl Diphosphatel. In J. Biochem (Vol. 114).